医疗器械|中国|医疗器械经营企业许可
认证网 (2012/11/21 18:58:57) 浏览:909 评论:0
《医疗器械监督管理条例》制定了在我国境内开办的医疗器械经营企业的许可制度:开办第I类医疗器械经营企业,应当向省、自治区、直辖市人民政府药品监督管理部门备案;开办第II类、第III类医疗器械经营企业,应当经省、自治区、直辖市人民政府药品监督管理部门审查批准,并发给《医疗器械经营企业许可证》。如果企业不能取得《医疗器械生产企业许可证》,将无法获得工商行政管理部门颁发的营业执照。《医疗器械经营企业许可证》有效期5年,有效期届满应当重新审查发证。医疗器械经营企业和医疗机构应从取得《医疗器械生产企业许可证》的生产企业或者取得《医疗器械经营企业许可证》的经营企业购进合格的医疗器械,并验明产品合格证明。医疗器械经营企业不得经营未经注册、无合格证明、过期、失效或者淘汰的医疗器械。
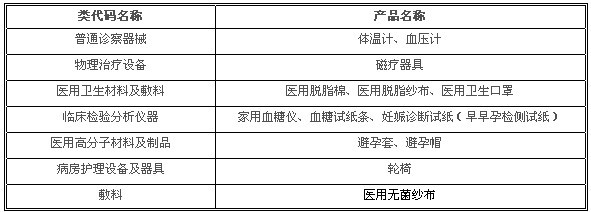
2004年6月25日,国家食品药品监督管理局颁布并实施了《医疗器械经营企业许可证管理办法》,对《条例》中有关医疗器械经营企业管理要求的内容进行了细化。该《管理办法》规定:在流通过程中通过常规管理能够保证其安全性、有效性的少数第II类医疗器械可以不申请《医疗器械经营企业许可证》。不需申请《医疗器械经营企业许可证》的第II类医疗器械产品名录由国家食品药品监督管理局制定。2005年5月,国家食品药品监督管理局公布了第一批不需申请《医疗器械经营企业许可证》的第II类医疗器械产品名录,共计7类13个产品,见下表:
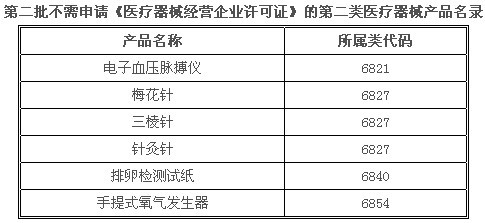
2011年11月,国家食药总局公布了第二批不需申请《医疗器械经营企业许可证》的第二类医疗器械产品名录。此次公布的名录,共6个产品。名录如下:
《医疗器械经营企业许可证管理办法》对申请“医疗器械经营企业许可证”的企业应当具备的条件做了具体规定:
具有与经营规模和经营范围相适应的质量管理机构或者专职质量管理人员。质量管理人员应当具有国家认可的相关专业学历或者职称;
具有与经营规模和经营范围相适应的相对独立的经营场所;
具有与经营规模和经营范围相适应的储存条件,包括具有符合医疗器械产品特性要求的储存设施、设备;
应当建立健全产品质量管理制度,包括采购、进货验收、仓储保管、出库复核、质量跟踪制度和不良事件的报告制度等;
应当具备与其经营的医疗器械产品相适应的技术培训和售后服务的能力,或者约定由第三方提供技术支持。
除此之外,该《管理办法》还制定了《医疗器械经营企业许可证》申请程序和对获证企业监督检查的详细要求。
2004年6月25日,国家食品药品监督管理局颁布并实施了《医疗器械经营企业许可证管理办法》,对《条例》中有关医疗器械经营企业管理要求的内容进行了细化。该《管理办法》规定:在流通过程中通过常规管理能够保证其安全性、有效性的少数第II类医疗器械可以不申请《医疗器械经营企业许可证》。不需申请《医疗器械经营企业许可证》的第II类医疗器械产品名录由国家食品药品监督管理局制定。2005年5月,国家食品药品监督管理局公布了第一批不需申请《医疗器械经营企业许可证》的第II类医疗器械产品名录,共计7类13个产品,见下表:
2011年11月,国家食药总局公布了第二批不需申请《医疗器械经营企业许可证》的第二类医疗器械产品名录。此次公布的名录,共6个产品。名录如下:
《医疗器械经营企业许可证管理办法》对申请“医疗器械经营企业许可证”的企业应当具备的条件做了具体规定:
具有与经营规模和经营范围相适应的质量管理机构或者专职质量管理人员。质量管理人员应当具有国家认可的相关专业学历或者职称;
具有与经营规模和经营范围相适应的相对独立的经营场所;
具有与经营规模和经营范围相适应的储存条件,包括具有符合医疗器械产品特性要求的储存设施、设备;
应当建立健全产品质量管理制度,包括采购、进货验收、仓储保管、出库复核、质量跟踪制度和不良事件的报告制度等;
应当具备与其经营的医疗器械产品相适应的技术培训和售后服务的能力,或者约定由第三方提供技术支持。
除此之外,该《管理办法》还制定了《医疗器械经营企业许可证》申请程序和对获证企业监督检查的详细要求。








